Inhaltsverzeechnes fir dësen Artikel:
1. Entwécklung vun Aminosaier Saieren
2. Strukturell Eegeschaften
3. Chemesch Zesummesetzung
4.Klassifikatioun
5. Synthese
6. Physiochemesch Eegeschaften
7. Toxizitéit
8. Antimikrobial Aktivitéit
9. Rheologesch Eegeschaften
10. Uwendungen an der Kosmetikindustrie
11. Uwendungen am Alldag Kosmetik
Aminosäure Surfaktanten (AAS)sinn eng Klass vun Surfaktanten geformt andeems hydrophobe Gruppen mat enger oder méi Aminosäuren kombinéiert ginn.An dësem Fall kënnen d'Aminosäuren synthetesch sinn oder aus Proteinhydrolysaten oder ähnlechen erneierbaren Quellen ofgeleet ginn.Dëse Pabeier deckt d'Detailer vun de meeschte verfügbare synthetesche Weeër fir AAS an den Effekt vu verschiddene Weeër op déi physikalesch-chemesch Eegeschafte vun den Endprodukter, dorënner Solubilitéit, Dispersiounsstabilitéit, Toxizitéit a Biodegradabilitéit.Als Klass vun Surfaktanten an der wuessender Nofro bitt d'Vielsäitegkeet vun AAS wéinst hirer verännerlecher Struktur eng grouss Zuel vu kommerziellen Méiglechkeeten.
Virausgesat datt Surfaktanten wäit an Detergenten, Emulgatoren, Korrosiounsinhibitoren, Tertiär Ueleg Erhuelung a Medikamenter benotzt ginn, hunn d'Fuerscher ni opgehalen op Surfaktanten opmierksam ze maachen.
Surfaktanten sinn déi representativst chemesch Produkter, déi alldeeglech a grousse Quantitéite ronderëm d'Welt verbraucht ginn an en negativen Impakt op d'aquatesch Ëmwelt hunn.Studien hu gewisen datt déi verbreet Notzung vun traditionellen Surfaktanten en negativen Impakt op d'Ëmwelt hunn.
Haut sinn Net-Toxizitéit, Biologesch Ofbaubarkeet a Biokompatibilitéit bal sou wichteg fir Konsumenten wéi d'Nëtzlechkeet an d'Leeschtung vun Surfaktanten.
Biosurfactants sinn ëmweltfrëndlech nohalteg Surfaktanten déi natierlech vu Mikroorganismen wéi Bakterien, Pilze an Hef synthetiséiert ginn, oder extrazellulär secretéiert ginn.Dofir kënnen Biosurfactanten och duerch molekulare Design virbereet ginn fir natierlech amphiphile Strukturen ze mimikéieren, sou wéi Phospholipiden, Alkylglycosiden an Acylaminosäuren.
Aminosäure Surfaktanten (AAS)sinn eng vun den typesche Surfaktanten, normalerweis aus Déieren oder landwirtschaftlech ofgeleet Matière première produzéiert.An de leschten zwee Joerzéngte hunn AAS vill Interessi vu Wëssenschaftler als nei Surfaktanten ugezunn, net nëmme well se aus erneierbaren Ressourcen synthetiséiert kënne ginn, awer och well AAS liicht ofbaubar sinn an harmlos Nebenprodukter hunn, wat se méi sécher mécht fir den Ëmwelt.
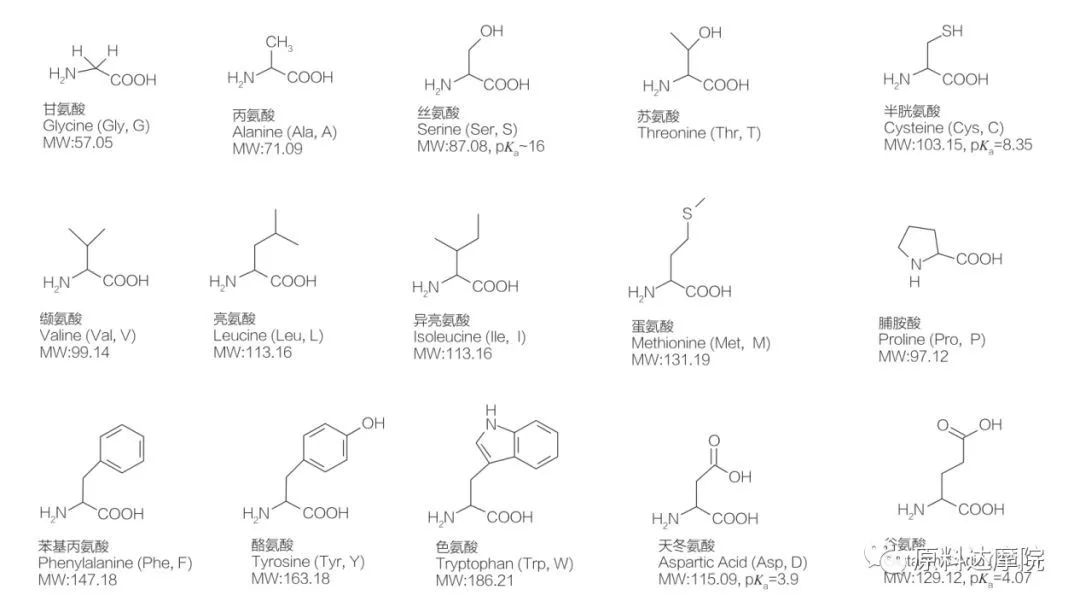
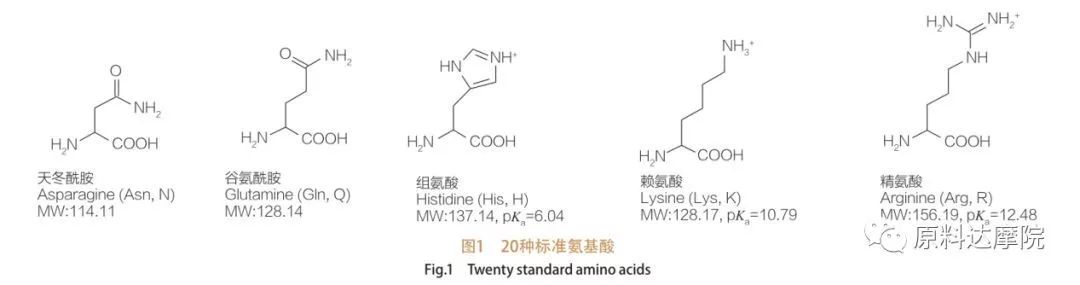
AAS kann als Klasse vun Surfaktanten definéiert ginn, déi aus Aminosäuren besteet, déi Aminosaiergruppen enthalen (HO 2 C-CHR-NH 2) oder Aminosaierreschter (HO 2 C-CHR-NH-).Déi 2 funktionell Regioune vun Aminosaieren erlaben d'Ofdreiwung vun enger grousser Varietéit vun Surfaktanten.Insgesamt 20 Standard Proteinogen Aminosaieren si bekannt fir an der Natur ze existéieren a si verantwortlech fir all physiologesch Reaktiounen am Wuesstum a Liewensaktivitéiten.Si ënnerscheede sech vuneneen nëmmen no dem Rescht R (Figur 1, pka ass den negativen Logarithmus vun der Säuredissoziatiounskonstant vun der Léisung).E puer sinn net-polar an hydrophob, e puer sinn polar an hydrophil, e puer sinn Basis an e puer si sauer.
Well Aminosäuren erneierbar Verbindunge sinn, hunn Surfaktanten, déi aus Aminosaieren synthetiséiert ginn, och e grousst Potenzial fir nohalteg an ëmweltfrëndlech ze ginn.Déi einfach an natierlech Struktur, geréng Toxizitéit a séier biologesch Ofbaubarkeet maachen se dacks super wéi konventionell Surfaktanten.Mat erneierbaren Rohmaterialien (zB Aminosäuren a Geméisueleg) kann AAS duerch verschidde biotechnologesch Weeër a chemesch Weeër produzéiert ginn.
Am fréien 20. Joerhonnert goufen Aminosäuren fir d'éischt entdeckt fir als Substrate fir d'Synthese vun Surfaktanten benotzt ze ginn.AAS goufen haaptsächlech als Konservéierungsmëttel a pharmazeuteschen a kosmetesche Formuléierungen benotzt.Zousätzlech goufen AAS fonnt fir biologesch aktiv géint eng Vielfalt vu Krankheet-verursaache Bakterien, Tumoren a Viren ze sinn.Am Joer 1988 huet d'Disponibilitéit vu Low-Cost AAS Fuerschungsinteresse fir Surface Aktivitéit generéiert.Haut, mat der Entwécklung vun der Biotechnologie, kënnen e puer Aminosäuren och kommerziell op enger grousser Skala duerch Hefe synthetiséiert ginn, wat indirekt beweist datt d'AAS Produktioun méi ëmweltfrëndlech ass.
01 Entwécklung vun Aminosaier Saieren
Schonn am fréien 19. Joerhonnert, wéi natierlech Aminosäuren fir d'éischt entdeckt goufen, goufen hir Strukture virausgesot extrem wäertvoll ze sinn - benotzbar als Rohmaterial fir d'Virbereedung vun Amphiphilen.Déi éischt Studie iwwer d'Synthese vun AAS gouf vum Bondi am Joer 1909 gemellt.
An där Studie goufen N-Acylglycin an N-Acylalanin als hydrophile Gruppe fir Surfaktanten agefouert.Déi spéider Aarbecht involvéiert d'Synthese vu LipoAminosäuren (AAS) mat Glycin an Alanin, an Hentrich et al.publizéiert eng Serie vu Resultater,inklusiv déi éischt Patentanmeldung, iwwer d'Benotzung vun Acylsarkosinat an Acylaspartatsalze als Surfaktanten an Haushaltsreinigungsprodukter (zB Shampoos, Detergenten an Zahnpasta).Duerno hunn vill Fuerscher d'Synthese an d'physikalesch-chemesch Eegeschafte vun Acylaminosäuren ënnersicht.Bis haut ass eng grouss Literatur iwwer d'Synthese, d'Eegeschafte, d'industriell Uwendungen an d'Biologesch Ofbaubarkeet vun AAS publizéiert ginn.
02 Strukturell Eegeschafte
Déi net-polare hydrophobe Fettsäurekette vun AAS kënnen an der Struktur, Kettelängt an Zuel variéieren.Déi strukturell Diversitéit an héich Uewerflächenaktivitéit vun AAS erklären hir breet Kompositiounsdiversitéit a physeschchemesch a biologesch Eegeschaften.D'Kappgruppen vun AAS besteet aus Aminosaieren oder Peptiden.D'Ënnerscheeder an de Kappgruppen bestëmmen d'Adsorptioun, d'Aggregatioun an d'biologesch Aktivitéit vun dësen Surfaktanten.Déi funktionell Gruppen an der Kappgruppe bestëmmen dann d'Aart vun AAS, dorënner kationesch, anionesch, nonionesch an amphoter.D'Kombinatioun vun hydrophilen Aminosaieren an hydrophobe laang Ketten Portiounen bilden eng amphiphil Struktur déi d'Molekül héich Uewerfläch aktiv mécht.Zousätzlech hëlleft d'Präsenz vun asymmetresche Kuelestoffatomer an der Molekül fir chiral Moleküle ze bilden.
03 Chemesch Zesummesetzung
All Peptiden a Polypeptide sinn d'Polymeriséierungsprodukter vun dëse bal 20 α-Proteinogenen α-Aminosäuren.All 20 α-Aminosäuren enthalen eng Carboxylsäure funktionell Grupp (-COOH) an eng Aminosaier funktionell Grupp (-NH 2), souwuel un déi selwecht tetrahedral α-Kuelestoff Atom verbonnen.Aminosäuren ënnerscheede sech vuneneen duerch déi verschidde R-Gruppen, déi un den α-Kuelestoff verbonne sinn (ausser fir Lycin, wou d'R-Grupp Waasserstoff ass.) D'R-Gruppen kënnen a Struktur, Gréisst a Ladung ënnerscheeden (Aciditéit, Alkalinitéit).Dës Differenzen bestëmmen och d'Léisbarkeet vun Aminosaieren am Waasser.
Aminosäuren si chiral (ausser Glycin) a sinn optesch aktiv vun der Natur well se véier verschidde Substituenten hunn, déi mam Alpha Kuelestoff verbonne sinn.Aminosäuren hunn zwou méiglech Konformatiounen;si sinn net iwwerlappende Spigelbilder vuneneen, trotz der Tatsaach, datt d'Zuel vun de L-Stereoisomeren däitlech méi héich ass.D'R-Grupp präsent a verschiddenen Aminosaieren (Phenylalanin, Tyrosin an Tryptophan) ass Aryl, wat zu enger maximaler UV-Absorptioun bei 280 nm féiert.Déi sauer α-COOH an d'Basis α-NH 2 an Aminosäuren si fäeg fir ze ioniséieren, a béid Stereoisomeren, egal wéi se sinn, konstruéieren d'Ioniséierungs Gläichgewiicht hei ënnen.
R-COOH ↔R-COO-+ H+
R-NH3+↔R-NH2+ H+
Wéi am Ioniséierungsgläichgewiicht uewen gewisen, Aminosäuren enthalen op d'mannst zwee schwaach sauer Gruppen;allerdéngs ass d'Carboxylgrupp vill méi sauer am Verglach zu der protonéierter Aminogrupp.pH 7.4, d'Carboxylgrupp ass deprotonéiert wärend d'Aminogrupp protonéiert ass.Aminosäuren mat net-ioniséierbare R Gruppen sinn elektresch neutral bei dësem pH a bilden zwitterion.
04 Klassifikatioun
AAS kann no véier Critèren klasséiert ginn, déi hei ënnendrënner beschriwwe ginn.
4.1 No der Origine
| No der Hierkonft kann AAS an 2 Kategorien opgedeelt ginn wéi follegt. ① Natural Kategorie E puer natierlech optrieden Verbindungen, déi Aminosäuren enthalen, hunn och d'Fäegkeet fir Uewerfläch / Interface Spannungen ze reduzéieren, an e puer iwwerschreiden souguer d'Effizienz vu Glykolipiden.Dës AAS sinn och als Lipopeptide bekannt.Lipopeptide sinn niddereg molekulare Gewiichtsverbindungen, normalerweis produzéiert vu Bacillus Arten.
Esou AAS ginn weider an 3 Ënnerklassen opgedeelt:Surfactin, Iturin a Fengycin.
|
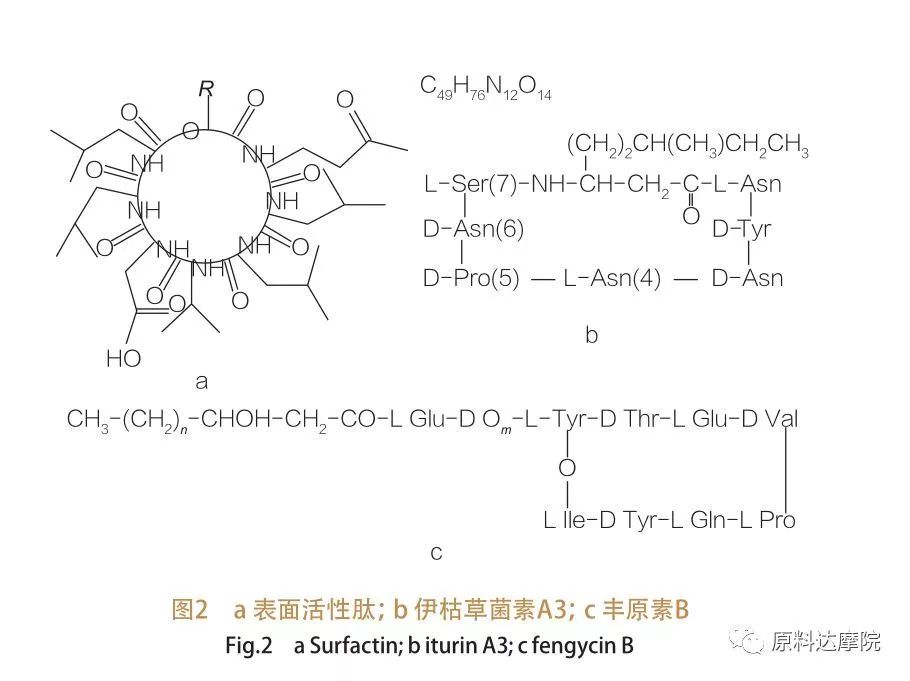
| D'Famill vun Uewerfläch-aktive Peptiden ëmfaasst heptapeptide Varianten vu verschiddene Substanzen,wéi an der Figur 2a gewisen, an där eng C12-C16 onsaturéiert β-Hydroxy Fettsäurekette mat dem Peptid verbonnen ass.Den Uewerfläch-aktive Peptid ass e makrozyklesche Lakton, an deem de Rank duerch Katalyse tëscht dem C-Terminus vun der β-Hydroxy-Fettsäure an dem Peptid zougemaach gëtt. An der Ënnerklass vum Iturin ginn et sechs Haaptvarianten, nämlech Iturin A a C, Mycosubtilin a Bacillomycin D, F a L.An alle Fäll sinn d'Heptapeptide mat den C14-C17 Ketten vun β-Amino Fettsäuren verbonnen (d'Ketten kënnen divers sinn).Am Fall vun den Ekurimycine kann d'Aminogrupp op der β-Positioun eng Amidebindung mam C-Terminus bilden, sou datt eng makrozyklesch Laktamstruktur bilden.
D'Ënnerklass Fengycin enthält Fengycin A a B, déi och Plipastatin genannt ginn wann Tyr9 D-konfiguréiert ass.Den Decapeptid ass mat enger C14-C18 gesättigte oder onsaturéierte β-Hydroxy Fettsäure Kette verbonnen.Strukturell ass Plipastatin och e makrozyklesche Lakton, deen eng Tyr Säitkette op der Positioun 3 vun der Peptidsekvens enthält an eng Esterbindung mam C-terminale Rescht bildt, sou datt eng intern Ringstruktur bilden (wéi de Fall fir vill Pseudomonas Lipopeptiden ass).
② Synthetesch Kategorie AAS kann och synthetiséiert ginn andeems ee vun de sauer, Basis an neutral Aminosäuren benotzt.Allgemeng Aminosäuren, déi fir d'Synthese vun AAS benotzt ginn, sinn Glutaminsäure, Serin, Prolin, Asparaginsäure, Glycin, Arginin, Alanin, Leucin, a Proteinhydrolysaten.Dës Ënnerklass vun Surfaktanten kann duerch chemesch, enzymatesch a chemoenzymatesch Methoden virbereet ginn;awer, fir d'Produktioun vun AAS, chemesch Synthes ass méi wirtschaftlech machbar.Allgemeng Beispiller enthalen N-Lauroyl-L-Glutaminsäure an N-Palmitoyl-L-Glutaminsäure.
|
4.2 Baséiert op aliphatesch Kettensubstituenten
Baséierend op den alifatesche Kettensubstituenten, kënnen Aminosäure-baséiert Surfaktanten an 2 Typen opgedeelt ginn.
No der Positioun vum Substituent
| ①N-ersat AAS An N-substituéierte Verbindungen gëtt eng Aminogrupp duerch eng lipophile Grupp oder eng Carboxylgrupp ersat, wat zu engem Verloscht vun der Basisheet resultéiert.dat einfachst Beispill vun N-substituéierten AAS sinn N-Acyl Aminosäuren, déi wesentlech anionesch Surfaktanten sinn.n-substituéiert AAS hunn eng Amidbindung tëscht den hydrophoben an hydrophilen Portiounen.D'Amidbindung huet d'Fäegkeet eng Waasserstoffbindung ze bilden, wat d'Degradatioun vun dësem Surfaktant an engem sauer Ëmfeld erliichtert, sou datt et biodegradéierbar ass.
②C-ersat AAS A C-substituéierte Verbindungen geschitt d'Substitutioun an der Carboxylgrupp (iwwer eng Amid- oder Esterbindung).Typesch C-substituéiert Verbindungen (zB Ester oder Amiden) si wesentlech kationesch Surfaktanten.
③N- a C-substituéiert AAS An dëser Aart vun Surfaktant sinn souwuel d'Amino- a Carboxylgruppen den hydrophilen Deel.Dës Zort ass wesentlech en amphotereschen Surfaktant. |
4.3 No der Zuel vun hydrophob Schwänz
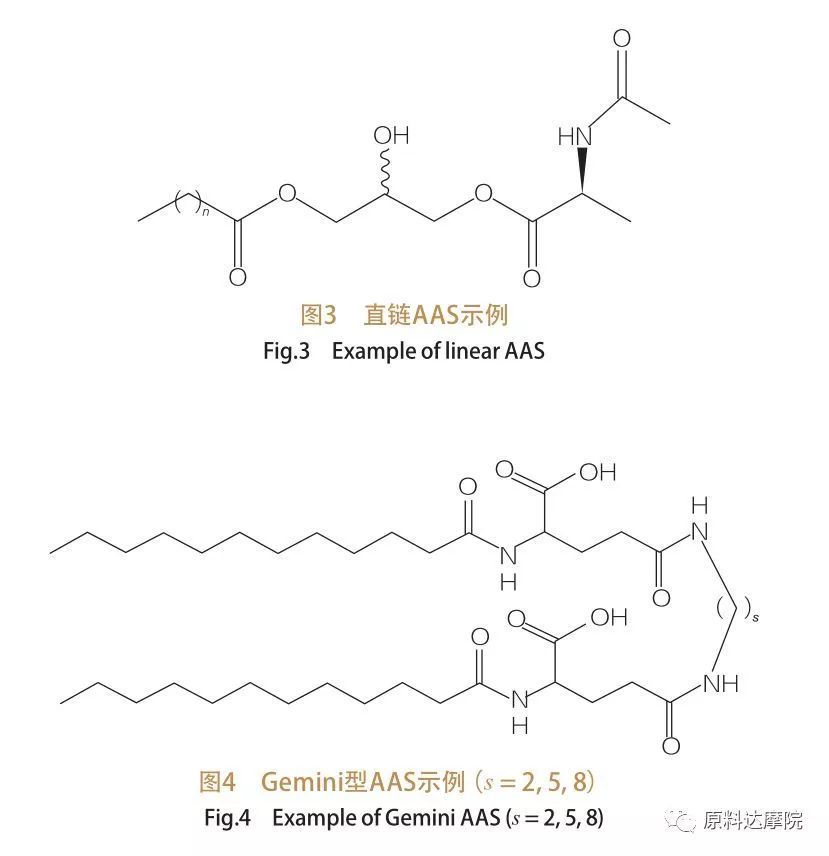
Baséierend op d'Zuel vu Kappgruppen an hydrophobesch Schwänz, kann AAS a véier Gruppen opgedeelt ginn.Riichtaus Kette AAS, Gemini (Dimer) Typ AAS, Glycerolipid Typ AAS, a bicephalic amphiphil (Bola) Typ AAS.riichtkette Surfaktanten sinn Surfaktanten, déi aus Aminosäuren mat nëmmen engem hydrophobesche Schwanz besteet (Figur 3).Gemini Typ AAS hunn zwou Aminosaier polare Kapp Gruppen an zwee hydrophob Schwänz pro Molekül (Figur 4).An dëser Aart vu Struktur sinn déi zwee riichtketten AAS matenee verbonne mat engem Spacer a ginn dofir och Dimer genannt.Am Glycerolipid Typ AAS, op der anerer Säit, sinn déi zwee hydrophobesch Schwänz un déiselwecht Aminosaier Kappgrupp befestegt.Dës Surfaktanten kënnen als Analoge vu Monoglyceriden, Diglyceriden a Phospholipiden ugesi ginn, wärend am Bola-Typ AAS zwou Aminosaier Kappgruppen duerch e hydrophobesche Schwanz verbonne sinn.
4.4 No der Zort Kapp Grupp
①Kationesch AAS
D'Kappgrupp vun dëser Zort Surfaktant huet eng positiv Ladung.Déi fréizäiteg kationesch AAS ass Ethylcocoylarginat, wat e Pyrrolidoncarboxylat ass.Déi eenzegaarteg an divers Eegeschafte vun dësem Surfaktant maachen et nëtzlech an Desinfektiounsmëttelen, antimikrobiellen Agenten, antistatesch Agenten, Hoerkonditioner, souwéi sanft op d'Aen an d'Haut a liicht biologesch ofbaubar.Singare a Mhatre synthetiséiert arginin-baséiert kationesch AAS an evaluéiert hir physeschchemesch Eegeschaften.An dëser Etude behaapten si héich Ausbezuelen vun de Produkter, déi mat Schotten-Baumann Reaktiounsbedéngungen kritt goufen.Mat enger Erhéijung vun der Alkylkettelängt an der Hydrophobitéit gouf d'Uewerflächenaktivitéit vum Surfaktant fonnt fir eropzegoen an d'kritesch Micelle Konzentratioun (cmc) ze reduzéieren.En aneren ass de quaternären Acylprotein, deen allgemeng als Conditioner an Hoerfleegprodukter benotzt gëtt.
②Anionesch AAS
An anionesche Surfaktanten huet d'polare Kappgrupp vum Surfaktant eng negativ Ladung.Sarcosin (CH 3 -NH-CH 2 -COOH, N-Methylglycin), eng Aminosäure déi allgemeng a Mierercher a Mierstäre fonnt gëtt, ass chemesch mat Glycin (NH 2 -CH 2 -COOH,) verbonnen, eng Basis Aminosäure déi fonnt gëtt. an Mamendéieren Zellen.-COOH,) ass chemesch mat Glycin verbonnen, wat eng Basis Aminosäure ass, déi a Mamendéierenzellen fonnt gëtt.Laurinsäure, Tetradekansäure, Olinsäure an hir Halogeniden an Ester ginn allgemeng benotzt fir sarcosinat Surfaktanten ze synthetiséieren.Sarcosinate sinn inherent mëll a ginn dofir allgemeng a Mondwäschen, Shampoos, Spray Raséierschaum, Sonneschutz, Hautreiniger an aner kosmetesch Produkter benotzt.
Aner kommerziell verfügbar anionesch AAS enthalen Amisoft CS-22 an AmiliteGCK-12, déi Handelsnumm fir Natrium N-Cocoyl-L-Glutamat a Kalium N-Cocoylglycinat sinn, respektiv.Amilite gëtt allgemeng als Schaummëttel, Detergent, Solubiliséierer, Emulgator an Dispergéierungsmëttel benotzt, an huet vill Uwendungen a Kosmetik, wéi Shampoos, Bad Seifen, Kierperwäschen, Zahnpasta, Gesiichtsreiniger, Reinigungsseifen, Kontaktlinsenreiniger an Haushalts Surfaktanten.Amisoft gëtt als mëll Haut- an Hoerreiniger benotzt, haaptsächlech a Gesiichts- a Kierperreiniger, blockéiert syntheteschen Detergenten, Kierperfleegprodukter, Shampoos an aner Hautpfleegprodukter.
③zwitterionesch oder amphoteresch AAS
Amphoteresch Surfaktanten enthalen souwuel sauer wéi och Basisplazen a kënnen dofir hir Ladung änneren andeems de pH-Wäert geännert gëtt.An alkalesche Medien behuelen se sech wéi anionesch Surfaktanten, wärend se an sauer Ëmfeld behuelen wéi kationesch Surfaktanten an an neutrale Medien wéi amphoteren Surfaktanten.Lauryl Lysin (LL) an Alkoxy (2-Hydroxypropyl) Arginin sinn déi eenzeg bekannt amphoteric surfactants baséiert op Aminosaier Saieren.LL ass e Kondensatiounsprodukt vu Lysin a Laurinsäure.Wéinst senger amphoterescher Struktur ass LL insoluble a bal all Zorte vu Léisungsmëttelen, ausser fir ganz alkalesch oder sauer Léisungsmëttel.Als organesch Pudder huet LL eng exzellent Adhäsioun op hydrophile Flächen an e gerénge Reibungskoeffizient, wat dësen Surfaktant exzellent Schmierfäegkeet gëtt.LL gëtt wäit an Hautcremen an Hoerkonditioner benotzt, a gëtt och als Schmierstoff benotzt.
④ Nonionesch AAS
Nonionesch Surfaktanten si charakteriséiert duerch polare Kappgruppen ouni formell Ladungen.aacht nei ethoxylated nonionic surfactants sech vun Al-Sabagh et al virbereet.aus Ueleglöslechen α-Aminosäuren.An dësem Prozess goufen L-Phenylalanin (LEP) a L-Leucin fir d'éischt mat Hexadecanol verestert, gefollegt vun der Amidatioun mat Palmitinsäure fir zwee Amiden an zwee Ester vun α-Aminosäuren ze ginn.D'Amiden an d'Ester hunn dann Kondensatiounsreaktiounen mat Ethylenoxid gemaach fir dräi Phenylalanin-Derivate mat verschiddenen Zuelen vu Polyoxyethylen-Eenheeten (40, 60 an 100) ze preparéieren.Dës nonionesch AAS goufen fonnt fir gutt Detergency a Schaumeigenschaften ze hunn.
05 Synthese
5.1 Basis syntheteschen Wee
An AAS kënnen hydrophobe Gruppen un Amin- oder Carboxylsäureplazen befestegt ginn, oder duerch d'Säiteketten vun Aminosaieren.Baséiert op dëser, véier Basis syntheteschen routes sinn disponibel, wéi an der Figur 5 gewisen.
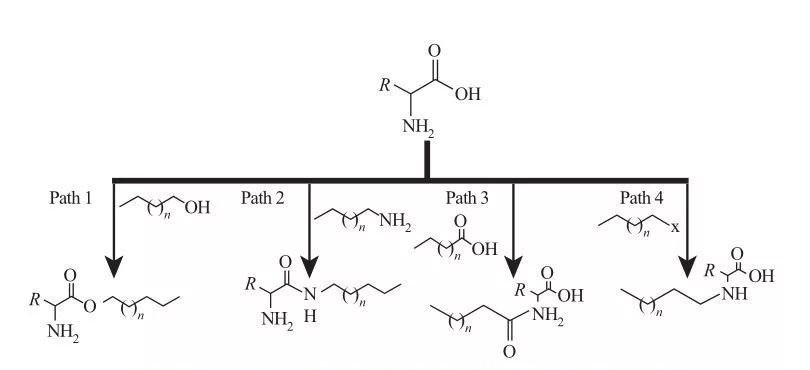
Fig.5 Fundamental Synthes Weeër vun Aminosaier-baséiert surfactants
| Wee 1. Amphiphile Esteramine ginn duerch Veresterungsreaktiounen produzéiert, an deem Fall gëtt d'Surfactant Synthese normalerweis erreecht duerch refluxéierend Fettalkoholen an Aminosäuren an der Präsenz vun engem Dehydratiounsmëttel an engem sauer Katalysator.A verschiddene Reaktiounen wierkt Schwefelsäure souwuel als Katalysator an als Dehydratiounsmëttel.
Wee 2. Aktivéiert Aminosäuren reagéieren mat Alkylaminen fir Amidbindungen ze bilden, wat zu der Synthese vun amphiphilen Amidoaminen resultéiert.
Wee 3. Amidosäuren ginn synthetiséiert andeems d'Amingruppen vun Aminosäuren mat Amidosäuren reagéieren.
Wee 4. Laangketten Alkyl Aminosäuren goufen duerch d'Reaktioun vun Amingruppen mat Haloalkanen synthetiséiert. |
5.2 Fortschrëtter an der Synthese an der Produktioun
5.2.1 Synthese vun Single-Chain Aminosaier / Peptid surfactants
N-Acyl oder O-Acyl Aminosäuren oder Peptiden kënne synthetiséiert ginn duerch enzymkatalyséiert Acylatioun vun Amin oder Hydroxylgruppen mat Fettsäuren.De fréierste Bericht iwwer d'Léisungsmëttelfräi Lipase-katalyséierter Synthese vun Aminosaieramid oder Methylester-Derivate benotzt Candida antarctica, mat Ausbezuele vu 25% bis 90% ofhängeg vun der Zil-Aminosäure.Methylethylketon gouf och als Léisungsmëttel an e puer Reaktiounen benotzt.Vonderhagen et al.beschriwwen och Lipase- a protease-katalyséiert N-Acylatiounsreaktiounen vun Aminosäuren, Proteinhydrolysaten an / oder hir Derivate mat enger Mëschung aus Waasser an organeschen Léisungsmëttelen (zB Dimethylformamid / Waasser) a Methylbutylketon.
An de fréie Deeg war den Haaptproblem mat enzymkatalyséierter Synthese vun AAS déi niddereg Ausbezuelen.Laut Valivety et al.d'Ausbezuele vun N-Tetradecanoyl Aminosaier Derivate war nëmmen 2% -10% och nodeems se verschidde Lipase benotzt hunn a vill Deeg bei 70 ° C inkubéiert.Montett et al.huet och Probleemer betreffend d'niddereg Ausbezuele vun Aminosäuren an der Synthese vun N-Acyl-Lysin mat Fettsäuren a Geméisueleg begéint.Laut hinnen war de maximale Rendement vum Produkt 19% ënner Léisungsmëttelfräi Bedéngungen a mat organesche Léisungsmëttelen.dee selwechte Problem huet Valivety et al.an der Synthese vun N-Cbz-L-Lysin oder N-Cbz-Lysin Methylester Derivate.
An dëser Etude hu si behaapt datt d'Ausbezuelung vun 3-O-Tetradecanoyl-L-Serine 80% war wann Dir N-geschützt Serin als Substrat benotzt an Novozyme 435 als Katalysator an engem geschmoltene Léisungsmëttelfräi Ëmfeld.Nagao a Kito hunn d'O-Acylatioun vu L-Serin, L-Homoserin, L-Threonin a L-Tyrosin (LET) studéiert wann Dir Lipase benotzt. a gemellt datt d'Ausbezuele vun der Acylatioun vu L-Homoserin a L-Serin e bëssen niddereg waren, während keng Acylatioun vu L-Threonin a LET geschitt ass.
Vill Fuerscher hunn d'Benotzung vu preiswerten a liicht verfügbare Substrate fir d'Synthese vu kosteneffizienten AAS ënnerstëtzt.Sou et al.behaapt datt d'Virbereedung vu Palmöl-baséiert Surfaktanten am beschten mat immobiliséierte Lipoenzym funktionnéiert.Si bemierken datt d'Ausbezuelung vun de Produkter trotz der Zäitopwänneg Reaktioun besser wier (6 Deeg).Gerova et al.ënnersicht d'Synthese an Uewerfläch Aktivitéit vun chiral N-Palmitoyl AAS baséiert op Methionin, Prolin, Leucin, Threonine, Phenylalanine an phenylglycine an enger cyclic / racemic Mëschung.Pang an Chu beschriwwen d'Synthese vun Aminosaier baséiert monomers an dicarboxylic sauerem baséiert monomers zu Léisung Eng Serie vun funktionell a biodegradable Aminosaier Saier-baséiert polyamide ester sech duerch Co-Kondensatioun Reaktioune an Léisung synthetiséiert.
Cantaeuzene a Guerreiro berichten d'Esterifikatioun vu Karboxylsäuregruppen vu Boc-Ala-OH a Boc-Asp-OH mat laangketten alifateschen Alkoholen an Diolen, mat Dichlormethan als Léisungsmëttel an Agarose 4B (Sepharose 4B) als Katalysator.An dëser Etude huet d'Reaktioun vu Boc-Ala-OH mat Fettalkoholen bis zu 16 Kuelestoffe gutt Ausbezuele ginn (51%), während fir Boc-Asp-OH 6 an 12 Kuelestoffe besser waren, mat enger entspriechender Ausbezuelung vun 63% [64] ].99,9%) an Ausbezuelen rangéiert vun 58% bis 76%, déi synthetiséiert goufen duerch d'Bildung vun Amidbindungen mat verschiddene laangketten Alkylaminen oder Esterbindungen mat Fettalkoholen duerch Cbz-Arg-OMe, wou Papain als Katalysator gehandelt huet.
5.2.2 Synthese vun Gemini-baséiert Aminosaier / Peptid surfactants
Aminosäure-baséiert Gemini Surfaktanten besteet aus zwee riichter Kette AAS Moleküle, déi Kapp-zu-Kapp matenee verbonne sinn duerch eng Spacer-Grupp.Et ginn 2 méiglech Schemae fir d'chemoenzymatesch Synthese vu Gemini-Typ Aminosaier-baséiert Surfaktanten (Figuren 6 a 7).An der Figur 6 ginn 2 Aminosaier Derivate mat der Verbindung als Spacer Grupp reagéiert an dann 2 hydrophobe Gruppen agefouert.An der Figur 7 sinn déi 2 riicht Kette Strukturen direkt matenee verbonne mat enger bifunktioneller Spacer Grupp.
Déi fréizäiteg Entwécklung vun der Enzym-katalyséierter Synthese vu Gemini Lipoaminosäuren gouf vu Valivety et al.Yoshimura et al.ënnersicht d'Synthese, d'Adsorptioun an d'Aggregatioun vun engem Aminosaier-baséierte Gemini Surfaktant baséiert op Cystin an n-Alkylbromid.Déi synthetiséiert Surfaktanten goufen mat den entspriechende monomeren Surfaktanten verglach.Faustino et al.beschreift d'Synthese vun anionesche Harnstoff-baséiert monomeren AAS baséiert op L-Cystin, D-Cystin, DL-Cystin, L-Cystein, L-Methionin a L-sulfoalanine an hir Pairen vun Gemini duerch Konduktivitéit, Gläichgewiicht Uewerflächespannung a stänneg -state fluorescence Charakteriséierung vun hinnen.Et gouf gewisen datt de cmc Wäert vu Gemini méi niddereg war andeems Monomer a Gemini vergläicht.
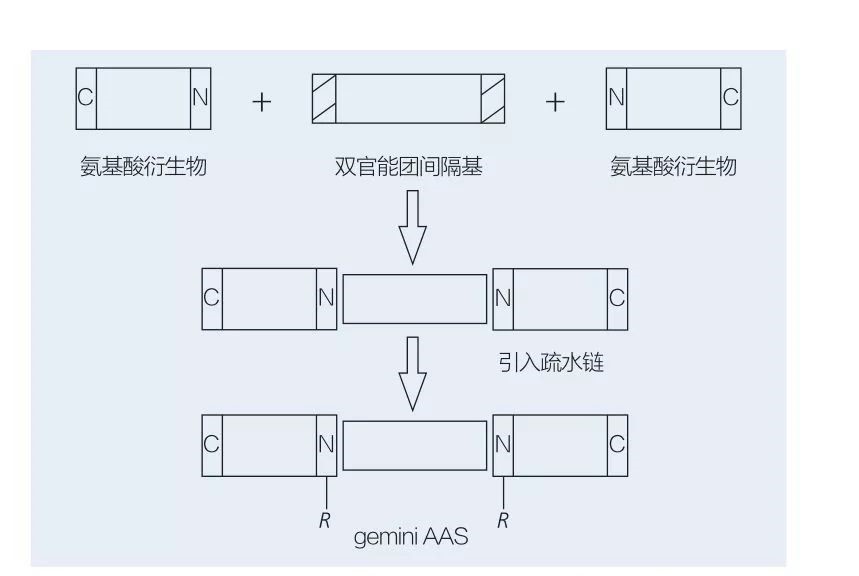
Fig.6 Synthese vu Gemini AAS mat AA Derivate a Spacer, gefollegt vun der Aféierung vun der hydrophobecher Grupp
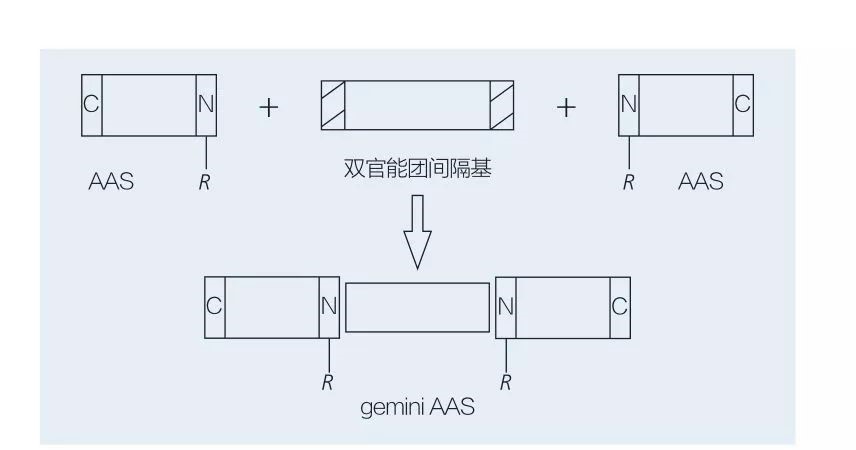
Fig.7 Synthes vun Gemini AAS benotzt bifunctional spacer an AAS
5.2.3 Synthese vu Glycerolipid Aminosaier/Peptid Surfaktanten
Glycerolipid Aminosaier / Peptid Surfaktanten sinn eng nei Klass vu Lipid Aminosaier Saieren déi strukturell Analoga vu Glycerol Mono- (oder Di-) Ester a Phospholipiden sinn, wéinst hirer Struktur vun enger oder zwou Fettketten mat enger Aminosäure verbonne mat der Glycerol Réckgrat duerch eng Esterbindung.D'Synthese vun dësen Surfaktanten fänkt mat der Preparatioun vu Glycerolester vun Aminosäuren bei erhéigen Temperaturen an a Präsenz vun engem sauer Katalysator (zB BF 3) un.Enzym-katalyséiert Synthese (mat Hydrolasen, Proteasen a Lipases als Katalysatoren) ass och eng gutt Optioun (Figur 8).
D'Enzym-katalyséiert Synthese vun dilauryléierten Argininglyceride Konjugaten mat Papain gouf gemellt.D'Synthese vun Diacylglycerolester Konjugaten aus Acetylarginin an d'Evaluatioun vun hire physikaleschen chemeschen Eegeschafte goufen och gemellt.
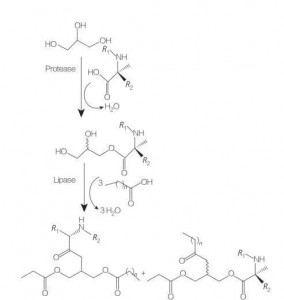
Fig.8 Synthese vu Mono- an Diacylglycerol Aminosaierkonjugaten
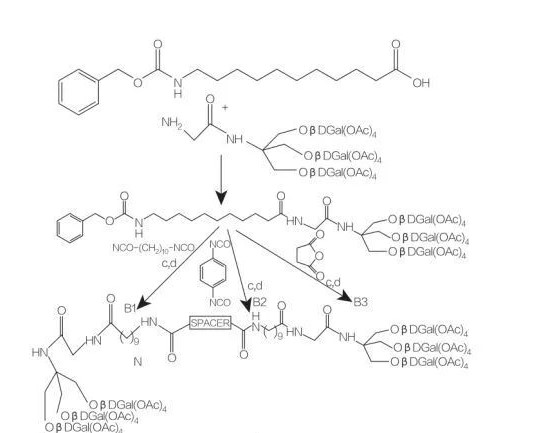
spacer: NH-(CH2)10-NH: VerbindungB1
spacer: NH-C6H4-NH: Verbindung B2
spacer: CH2-CH2: VerbindungB3
Fig.9 Synthese vu symmetresche Amphiphilen ofgeleet vum Tris(Hydroxymethyl)aminomethan
5.2.4 Synthese vu Bola-baséiert Aminosaier / Peptid Surfaktanten
Aminosaier-baséiert Bola-Typ Amphiphile enthalen 2 Aminosäuren, déi mat der selwechter hydrophobescher Kette verbonne sinn.Franceschi et al.beschreift d'Synthese vu Bola-Typ Amphiphilen mat 2 Aminosäuren (D- oder L-Alanin oder L-Histidin) an 1 Alkylkette vu verschiddene Längt an ënnersicht hir Uewerflächenaktivitéit.Si diskutéieren d'Synthese an d'Aggregatioun vun neie Bola-Typ Amphiphile mat enger Aminosäurefraktioun (benotzt entweder eng ongewéinlech β-Aminosäure oder en Alkohol) an enger C12 -C20 Spacer Grupp.Déi ongewéinlech β-Aminosäuren, déi benotzt ginn, kënnen eng Zocker Aminosäure, eng Azidothymin (AZT) ofgeleet Aminosaier, eng Norbornen Aminosaier, an en Aminoalkohol ofgeleet vun AZT sinn (Figur 9).d'Synthese vu symmetresche Bola-Typ Amphiphilen ofgeleet aus Tris(Hydroxymethyl)aminomethan (Tris) (Figur 9).
06 Physikalesch chemesch Eegeschaften
Et ass bekannt datt Aminosäure-baséiert Surfaktanten (AAS) divers a villsäiteg an der Natur sinn an eng gutt Uwendung a villen Uwendungen hunn wéi gutt Solubiliséierung, gutt Emulgéierungseigenschaften, héich Effizienz, héich Uewerflächeaktivitéit Leeschtung a gutt Resistenz géint hart Waasser (Kalziumion) Toleranz).
Baséierend op den Surfaktanteigenschaften vun Aminosaieren (zB Uewerflächespannung, cmc, Phaseverhalen a Krafft-Temperatur), goufen déi folgend Conclusiounen no extensiv Studien erreecht - d'Uewerflächenaktivitéit vun AAS ass superieur wéi déi vu sengem konventionellen Surfaktant-Kollegen.
6.1 Kritesch Mizelle Konzentratioun (cmc)
Kritesch Mizelle Konzentratioun ass ee vun de wichtege Parameteren vun surfactants a regéiert vill Uewerfläch aktiv Eegeschafte wéi Solubilization, Zell lysis a seng Interaktioun mat Biofilms, etc.. Am Allgemengen, Erhéijung vun der Kette Längt vun der Kuelewaasserstoff Schwäif (Erhéijung hydrophobicity) féiert zu enger Ofsenkung am cmc-Wäert vun der Surfaktantléisung, sou datt seng Uewerflächenaktivitéit erhéicht gëtt.Surfaktanten baséiert op Aminosäuren hunn normalerweis méi niddereg cmc Wäerter am Verglach mat konventionellen Surfaktanten.
Duerch verschidde Kombinatioune vu Kappgruppen a hydrophobe Schwänz (monokationesch Amid, bi-kationesch Amid, bi-kationesch Amide-baséiert Ester), Infante et al.synthetiséiert dräi arginine-baséiert AAS an studéiert hir cmc an γcmc (Uewerflächespannung bei cmc), weist datt d'cmc an γcmc Wäerter erofgaange sinn mat der Erhéijung vun der hydrophobesch Schwanzlängt.An enger anerer Studie hunn Singare a Mhatre festgestallt datt de cmc vun N-α-Acylarginin-Surfaktanten erofgaang ass mat der Erhéijung vun der Unzuel vun hydrophobesche Schwanzkuelestoffatome (Table 1).
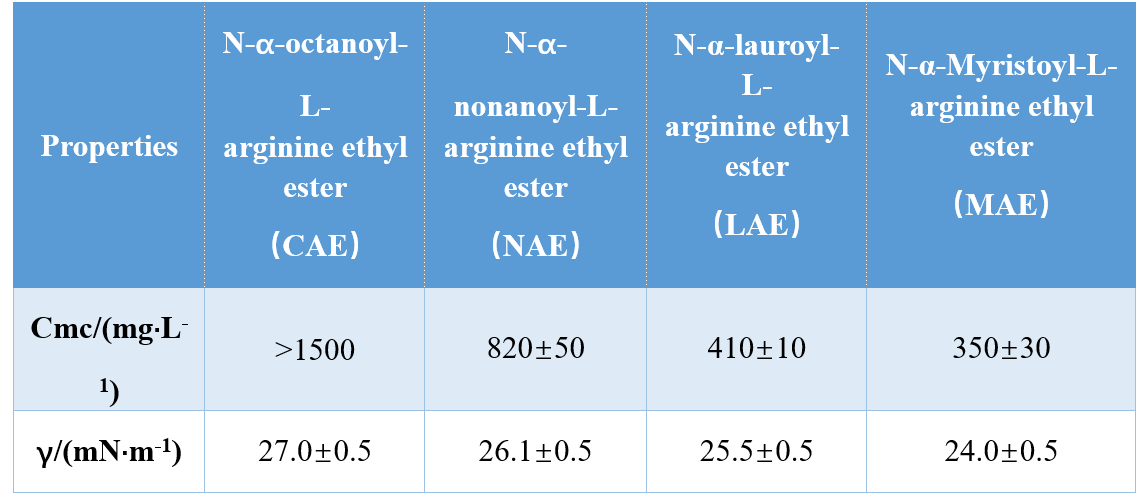
Yoshimura et al.ënnersicht de cmc vun cysteine-ofgeleet Aminosaier Saier-baséiert gemini surfactants a gewisen, datt de cmc ofgeholl wann d'Kuelestoff Kette Längt an der hydrophobic Kette vun 10 op 12 erhéicht gouf. déi bestätegt datt laangkette Gemini Surfaktanten eng méi niddereg Tendenz hunn ze aggregéiert.
Faustino et al.bericht d'Bildung vu gemëschte Mizellen an wässerleche Léisungen vun anionesche Gemini Surfaktanten op Basis vu Cystin.D'gemini surfactants sech och mat der entspriechend konventionell monomeric surfactants (C 8 Cys) Verglach.D'cmc Wäerter vu Lipid-Surfactant Mëschunge goufen gemellt manner ze sinn wéi déi vu pure Surfactant.Gemini Surfaktanten an 1,2-Diheptanoyl-sn-Glyceryl-3-Phosphocholin, e Waasserlöslechen, Mizellbildende Phospholipid, haten cmc am millimolare Niveau.
Shrestha an Aramaki ënnersicht d'Bildung vu viskoelastesche Wurm-ähnlechen Mizellen an wässerleche Léisunge vu gemëschten Aminosäure-baséiert anionesch-nonionesche Surfaktanten an der Verontreiung vun Zousatzsalze.An dëser Etude gouf N-dodecyl glutamate fonnt eng méi héich Krafft Temperatur ze hunn;awer, wann neutraliséiert mat der Basis Aminosaier L-Lysine, et generéiert Mizellen an der Léisung ugefaang wéi eng Newtonian Flëssegket bei 25 ° C ze behuelen.
6.2 Gutt Waasserléislechkeet
Déi gutt Waasserléislechkeet vun AAS ass wéinst der Präsenz vun zousätzlech CO-NH Obligatiounen.Dëst mécht AAS méi biodegradéierbar an ëmweltfrëndlech wéi déi entspriechend konventionell Surfaktanten.D'Waasserléislechkeet vun N-Acyl-L-Glutaminsäure ass nach besser wéinst senge 2 Carboxylgruppen.D'Waasserléislechkeet vu Cn(CA) 2 ass och gutt well et 2 ionesch Arginingruppen an 1 Molekül sinn, wat zu méi effektiver Adsorptioun an Diffusioun op der Zell-Interface a souguer effektiv bakteriell Hemmung bei méi nidderegen Konzentratioune resultéiert.
6.3 Kraffttemperatur an Krafftpunkt
Krafft Temperatur kann als spezifescht Solubilitéitsverhalen vun Surfaktanten verstane ginn, deenen hir Solubilitéit staark iwwer eng bestëmmten Temperatur eropgeet.Ionesch Surfaktanten hunn eng Tendenz fir fest Hydrate ze generéieren, déi aus Waasser ausfälle kënnen.Bei enger bestëmmter Temperatur (déi sougenannte Krafft-Temperatur) gëtt normalerweis eng dramatesch an diskontinuéierlech Erhéijung vun der Solubilitéit vun Surfaktanten beobachtet.De Krafftpunkt vun engem ionesche Surfaktant ass seng Kraffttemperatur bei cmc.
Dës Solubilitéitskarakteristik ass normalerweis fir ionesch Surfaktanten ze gesinn a kann esou erkläert ginn: d'Léislechkeet vum Surfaktant-fräie Monomer ass ënner der Kraffttemperatur limitéiert bis de Krafft-Punkt erreecht gëtt, wou seng Solubilitéit duerch Mizellebildung graduell eropgeet.Fir komplett Solubilitéit ze garantéieren, ass et néideg Surfaktant Formuléierungen bei Temperaturen iwwer dem Krafftpunkt ze preparéieren.
D'Kraffttemperatur vun AAS gouf studéiert a verglach mat där vun konventionelle syntheteschen Surfaktanten.Shrestha an Aramaki hunn d'Krafttemperatur vun Arginin-baséiert AAS studéiert a fonnt datt déi kritesch Mizellekonzentratioun Aggregatiounsverhalen a Form vu Pre-Mizellen iwwer 2-5 huet. ×10-6 mol-L -1 gefollegt vun der normaler Mizellebildung (Ohta et al. Synthetiséiert sechs verschidden Aarte vun N-Hexadecanoyl AAS an diskutéiert d'Relatioun tëscht hirer Kraffttemperatur an Aminosaierreschter.
An den Experimenter gouf festgestallt datt d'Krafttemperatur vun N-Hexadecanoyl AAS eropgeet mat erofgaangener Gréisst vun Aminosäurereschter (Phenylalanin ass eng Ausnahm), während d'Hëtzt vun der Solubilitéit (Wärmeaufnahme) eropgeet mat erofgaangener Gréisst vun Aminosaierreschter (mat Ausnam vu Glycin a Phenylalanin).Et gouf ofgeschloss datt a béid Alanin a Phenylalanin Systemer d'DL Interaktioun méi staark ass wéi d'LL Interaktioun an der fester Form vum N-Hexadecanoyl AAS Salz.
Brito et al.huet d'Kraffttemperatur vun dräi Serien vun neien Aminosaier-baséierten Surfaktanten mat Differential-Scannen-Mikrokalorimetrie bestëmmt a festgestallt datt d'Verännerung vum Trifluoracetat-Ion op Jodid-Ion zu enger wesentlecher Erhéijung vun der Krafft-Temperatur (ongeféier 6 °C), vu 47 °C op 53 °C gefouert huet. C.D'Präsenz vu cis-Duebelbindungen an d'Onsaturatioun, déi an de laangketten Ser-Derivate präsent ass, hunn zu enger wesentlecher Ofsenkung vun der Kraffttemperatur gefouert.n-Dodecyl glutamate gouf gemellt eng méi héich Krafft Temperatur ze hunn.Wéi och ëmmer, Neutraliséierung mat der Basis Aminosaier L-Lysin huet zu der Bildung vu Mizellen a Léisung gefouert, déi sech wéi Newtonesch Flëssegkeete bei 25 ° C behuelen.
6.4 Uewerflächespannung
D'Uewerflächespannung vun Surfaktanten ass mat der Kettelängt vum hydrophoben Deel verbonnen.Zhang et al.bestëmmt d'Uewerflächespannung vum Natriumcocoylglycinat duerch d'Wilhelmy-Plackmethod (25±0,2)°C an huet d'Uewerflächespannungswäert bei cmc als 33 mN-m -1, cmc als 0,21 mmol-L -1 bestëmmt.Yoshimura et al.bestëmmt d'Uewerflächespannung vun 2C n Cys Typ Aminosaier Uewerfläch Uewerfläch Spannung vun 2C n Cys-baséiert Uewerfläch aktiv Agenten.Et gouf festgestallt datt d'Uewerflächespannung bei cmc mat der Erhéijung vun der Kettelängt erofgaang ass (bis n = 8), während den Trend fir Surfaktanten mat n = 12 oder méi laang Kettenlängt ëmgedréit gouf.
Den Effekt vu CaC1 2 op d'Uewerflächespannung vun dicarboxyléierten Aminosaier-baséierten Surfaktanten ass och studéiert ginn.An dëse Studien gouf CaC1 2 zu wässerleche Léisungen vun dräi dicarboxyléiert Aminosaier-Typ Surfaktanten (C12 MalNa 2, C12 AspNa 2, an C12 GluNa 2) bäigefüügt.D'Plateauwäerter no cmc goufen verglach an et gouf festgestallt datt d'Uewerflächespannung bei ganz nidderegen CaC1 2 Konzentratioune erofgaang ass.Dëst ass wéinst dem Effekt vu Kalziumionen op d'Arrangement vum Surfaktant um Gas-Waasser-Interface.d'Uewerflächespannunge vun de Salze vun N-dodecylaminomalonate an N-dodecylaspartate, op der anerer Säit, waren och bal konstant bis zu 10 mmol-L -1 CaC1 2 Konzentratioun.Iwwer 10 mmol-L -1 klëmmt d'Uewerflächespannung staark, duerch d'Bildung vun enger Nidderschlag vum Kalziumsalz vum Surfaktant.Fir den Dinatriumsalz vum N-Dodecyl-Glutamat huet moderéiert Zousatz vu CaC1 2 zu enger wesentlecher Ofsenkung vun der Uewerflächespannung gefouert, während eng weider Erhéijung vun der CaC1 2 Konzentratioun net méi bedeitend Ännerungen verursaacht huet.
Fir d'Adsorptiounskinetik vum Gemini-Typ AAS op der Gas-Waasser-Interface ze bestëmmen, gouf déi dynamesch Uewerflächespannung mat der maximaler Blasendruckmethod bestëmmt.D'Resultater weisen datt fir déi längsten Testzäit d'2C 12 Cys dynamesch Uewerflächespannung net geännert huet.D'Ofsenkung vun der dynamescher Uewerflächespannung hänkt nëmmen vun der Konzentratioun, der Längt vun den hydrophobesche Schwänz an der Unzuel vun de hydrophobesche Schwänz of.D'Erhéijung vun der Konzentratioun vum Surfaktant, d'Kettelängt erofgoen, souwéi d'Zuel vun de Ketten huet zu engem méi séieren Zerfall gefouert.D'Resultater, déi fir méi héich Konzentratioune vu C n Cys (n = 8 bis 12) kritt goufen, ware ganz no beim γ cmc gemooss vun der Wilhelmy Method fonnt.
An enger anerer Etude, déi dynamesch Uewerfläch Spannungen vun Natrium dilauryl cystine (SDLC) an Natrium didecamino cystine goufen duerch d'Wilhelmy Platte Method bestëmmt, an zousätzlech, d'Gläichgewiicht Uewerfläch Spannungen vun hire wässerlech Léisungen goufen duerch d'Drëpsvolumen Method bestëmmt.D'Reaktioun vun Disulfidbindunge gouf och mat anere Methoden ënnersicht.D'Zousatz vu Mercaptoethanol zu 0,1 mmol-L -1SDLC Léisung huet zu enger séierer Erhéijung vun der Uewerflächespannung vu 34 mN-m -1 op 53 mN-m -1 gefouert.Well NaClO d'Disulfidbindunge vun SDLC zu Sulfonsäuregruppen oxidéiere kann, goufen keng Aggregater observéiert wann NaClO (5 mmol-L -1) an d'0,1 mmol-L -1 SDLC Léisung bäigefüügt gouf.Transmissiounselektronenmikroskopie an dynamesch Liichtstreetresultater weisen datt keng Aggregaten an der Léisung geformt goufen.D'Uewerflächespannung vum SDLC gouf fonnt fir vun 34 mN-m -1 op 60 mN-m -1 iwwer eng Period vun 20 min ze erhéijen.
6.5 Binär Uewerfläch Interaktiounen
An de Liewenswëssenschaften hunn eng Rei vu Gruppen d'Schwéngungseigenschaften vu Mëschunge vu kationeschen AAS (Diacylglycerol Arginin-baséiert Surfaktanten) a Phospholipiden an der Gas-Waasser-Interface studéiert, schlussendlech ofgeschloss datt dës net-ideal Eegeschafte d'Prévalenz vun elektrostateschen Interaktiounen verursaacht.
6.6 Aggregatioun Eegeschafte
Dynamesch Liichtstreet gëtt allgemeng benotzt fir d'Aggregatiounseigenschaften vun Aminosäure-baséiert Monomeren a Gemini Surfaktanten bei Konzentratioune iwwer cmc ze bestëmmen, wat e scheinbar hydrodynameschen Duerchmiesser DH (= 2R H ) kritt.D'Aggregate geformt vu C n Cys an 2Cn Cys si relativ grouss an hunn eng breet Skala Verdeelung am Verglach mat anere Surfaktanten.All Surfaktanten ausser 2C 12 Cys bilden typesch Aggregate vun ongeféier 10 nm.Mizellegréisste vu Gemini Surfaktanten si wesentlech méi grouss wéi déi vun hire monomere Kollegen.Eng Erhéijung vun der Kuelewaasserstoffkettelängt féiert och zu enger Erhéijung vun der Mizellegréisst.op et al.beschriwwen d'Aggregatiounseigenschaften vun dräi verschiddene Stereoisomere vun N-Dodecyl-Phenyl-Alanyl-Phenyl-Alanine-Tetramethylammonium an der wässerlecher Léisung a weist datt d'Diastereoisomeren déiselwecht kritesch Aggregatiounskonzentratioun an der wässerlecher Léisung hunn.Iwahashi et al.ënnersicht duerch kreesfërmeg dichroism, NMR an Dampdruck Osmometry d'Bildung vu chiralen Aggregaten vun N-dodecanoyl-L-glutaminsäure, N-dodecanoyl-L-valin an hir Methylester a verschiddene Léisungsmëttelen (wéi Tetrahydrofuran, Acetonitril, 1,4) -Dioxan an 1,2-Dichlorethan) mat Rotatiounseigenschaften gouf duerch kreesfërmeg Dikroismus, NMR a Dampdruckosmometrie ënnersicht.
6.7 Interface Adsorptioun
D'Interfacial Adsorptioun vun Aminosaier-baséiert Surfaktanten a säi Verglach mat sengem konventionelle Kolleg ass och eng vun de Fuerschungsrichtungen.Zum Beispill goufen d'Interfacial Adsorptiounseigenschaften vun Dodecylester vun aromatesche Aminosäuren aus LET a LEP ënnersicht.D'Resultater weisen datt LET an LEP méi niddereg Interfaceflächen um Gas-Flësseg-Interface respektiv um Waasser / Hexan-Interface weisen.
Bordes et al.ënnersicht d'Léisungsverhalen an d'Adsorptioun um Gas-Waasser-Interface vun dräi dicarboxyléiert Aminosaier Surfaktanten, den Dinatriumsalze vun Dodecyl-Glutamat, Dodecyl-Aspartat, an Aminomalonat (mat 3, 2, an 1 Kuelestoffatomer tëscht den zwou Carboxylgruppen, respektiv).Laut dësem Bericht war de cmc vun den dicarboxyléierten Surfaktanten 4-5 Mol méi héich wéi dee vum monocarboxyléierten Dodecylglycin Salz.Dëst gëtt un d'Bildung vu Waasserstoffbindungen tëscht den dicarboxyléierten Surfaktanten an de Nopeschmolekülen duerch d'Amidegruppen doran zougeschriwwen.
6.8 Phase Verhalen
Isotrop diskontinuéierlech kubesch Phasen gi fir Surfaktanten bei ganz héije Konzentratioune beobachtet.Surfaktant Moleküle mat ganz grousse Kappgruppen tendéieren Aggregate vu méi klenger positiver Krümmung ze bilden.marques et al.studéiert d'Phaseverhalen vun den 12Lys12/12Ser- an 8Lys8/16Ser-Systemer (kuckt Figur 10), an d'Resultater weisen datt de 12Lys12/12Ser-System eng Phase-Trennungszon tëscht de micellare a vesikuläre Léisungsregiounen huet, während de 8Lys8/16Ser System. 8Lys8 / 16Ser System weist eng kontinuéierlech Transitioun (verlängerten micellar Phase Regioun tëscht der kleng micellar Phase Regioun an der vesicle Phase Regioun).Et sollt bemierkt datt fir d'Vesikelregioun vum 12Lys12 / 12Ser System, Vesikel ëmmer mat Mizellen existéieren, während d'Vesikelregioun vum 8Lys8 / 16Ser System nëmme Vesikel huet.
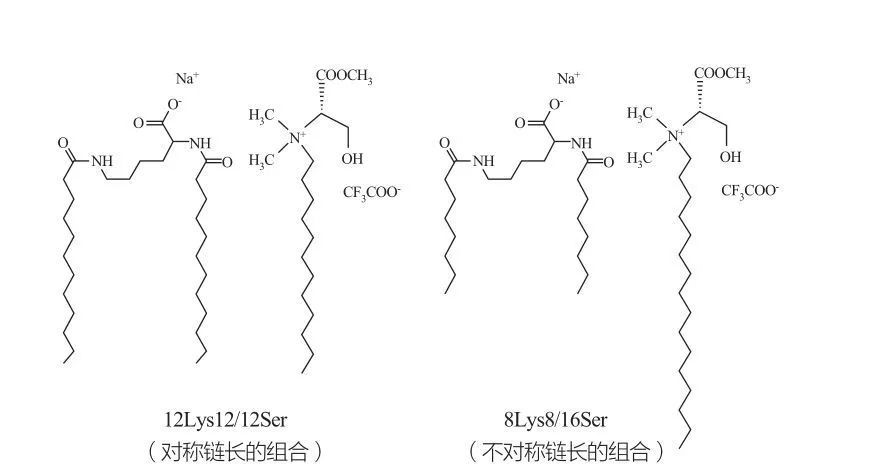
Katanionesch Mëschunge vun de Lysin- a Serin-baséiert Surfaktanten: symmetresch 12Lys12/12Ser Pair (lénks) an asymmetresch 8Lys8/16Ser Pair (riets)
6.9 Emulgéieren Fäegkeet
Kouchi et al.iwwerpréift d'Emulgéierungsfäegkeet, d'Interfacial Spannung, d'Dispergabilitéit an d'Viskositéit vun N-[3-Dodecyl-2-Hydroxypropyl]-L-Arginin, L-Glutamat, an aner AAS.Am Verglach mat syntheteschen Surfaktanten (hir konventionell netionesch an amphoteresch Géigeparteien), hunn d'Resultater gewisen datt AAS méi staark Emulgéierungsfäegkeet hunn wéi konventionell Surfaktanten.
Baczko et al.synthetiséiert nei anionesch Aminosaier Surfaktanten an ënnersicht hir Eegenheet als chiral orientéiert NMR Spektroskopie Léisungsmëttel.Eng Serie vu Sulfonat-baséiert amphiphilen L-Phe oder L-Ala Derivate mat verschiddene hydrophobe Schwänz (Pentyl~Tetradecyl) goufen synthetiséiert andeems Aminosäuren mat o-sulfobenzoic Anhydrid reagéieren.Wu et al.synthetiséiert Natriumsalze vun N-Fettacyl AAS anhunn hir Emulgéierungsfäegkeet an Ueleg-an-Waasser-Emulsiounen ënnersicht, an d'Resultater weisen datt dës Surfaktanten besser mat Ethylacetat als Uelegphase gemaach hunn wéi mat n-Hexan als Uelegphase.
6.10 Fortschrëtter an der Synthese an der Produktioun
Hard Waasserresistenz kann verstane ginn als d'Fäegkeet vun Surfaktanten fir d'Präsenz vun Ionen wéi Kalzium a Magnesium am hart Waasser ze widderstoen, dh d'Fäegkeet fir Nidderschlag a Kalziumseifen ze vermeiden.Surfaktanten mat héijer hart Waasserresistenz si ganz nëtzlech fir Detergentformuléierungen a perséinlech Betreiungsprodukter.Hard Waasserresistenz kann evaluéiert ginn andeems d'Verännerung vun der Solubilitéit an der Uewerflächenaktivitéit vum Surfaktant an der Präsenz vu Kalziumionen berechent gëtt.
Eng aner Manéier fir haart Waasserresistenz ze evaluéieren ass de Prozentsaz oder Gramm Surfaktant ze berechnen fir d'Kalziumseife geformt aus 100 g Natriumoleat a Waasser ze verdeelen.A Gebidder mat héijer haart Waasser, héich Konzentratioune vu Kalzium a Magnesiumionen a Mineralgehalt kënnen e puer praktesch Uwendunge schwéier maachen.Dacks gëtt den Natriumion als Konterion vun engem syntheteschen anionesche Surfaktant benotzt.Zënter datt dat zweewäertegt Kalziumion u béid Surfaktantmoleküle gebonnen ass, verursaacht et datt den Surfaktant méi einfach aus der Léisung ausfällt, wat d'Wäschmëttel manner wahrscheinlech mécht.
D'Studie vun der haart Waasser Resistenz vun AAS huet gewisen, datt d'Sauer an haart Waasser Resistenz staark vun enger zousätzlech Carboxyl Grupp beaflosst goufen, an der Seier an haart Waasser Resistenz weider mat der Erhéijung vun der Längt vun der Spacer Grupp tëscht den zwou Carboxyl Gruppen erop. .D'Uerdnung vu Säure- a schwéier Waasserresistenz war C 12 Glycinat < C 12 Aspartat < C 12 Glutamat.Am Verglach vun der dicarboxyléierter Amidebindung an dem dicarboxyléierten Amino-Surfactant, respektiv, gouf festgestallt datt de pH-Bereich vun der leschter méi breet war a seng Uewerflächeaktivitéit erhéicht mat der Zousatz vun enger passender Quantitéit Säure.D'dicarboxylated N-alkyl Aminosaier Saieren weisen chelating Effekt an der Präsenz vun Kalzium Ionen, an C 12 Aspartat geformt wäiss gelies.c 12 glutamate huet héich Uewerfläch Aktivitéit bei héich Ca 2+ Konzentratioun gewisen a gëtt erwaart an Mierwaasser desalination benotzt ginn.
6.11 Dispersibilitéit
Dispersibilitéit bezitt sech op d'Fäegkeet vun engem Surfaktant fir Koaleszenz a Sedimentatioun vum Surfaktant a Léisung ze vermeiden.Dispersibilitéit ass eng wichteg Eegeschafte vun Surfaktanten, déi se gëeegent mécht fir an Detergenten, Kosmetik a Medikamenter ze benotzen.En Dispergéierungsmëttel muss en Ester, Ether, Amid oder Aminobindung tëscht der hydrophobescher Grupp an der terminaler hydrophiler Grupp (oder ënner de riichter Kette hydrophobe Gruppen) enthalen.
Allgemeng sinn anionesch Surfaktanten wéi Alkanolamidosulfate an amphotere Surfaktanten wéi Amidosulfobetain besonnesch effektiv als Dispergéierungsmëttel fir Kalziumseifen.
Vill Fuerschungsefforten hunn d'Dispersibilitéit vun AAS festgeluegt, wou N-Lauroyl-Lysin fonnt gouf schlecht mat Waasser kompatibel ze sinn a schwéier fir kosmetesch Formuléierungen ze benotzen.An dëser Serie hunn N-acyl-substituéiert Basis Aminosäuren eng super Dispersibilitéit a ginn an der Kosmetikindustrie benotzt fir Formuléierungen ze verbesseren.
07 Toxizitéit
Konventionell Surfaktanten, besonnesch kationesch Surfaktanten, sinn héich gëfteg fir Waasserorganismen.Hir akuter Toxizitéit ass wéinst dem Phänomen vun der Adsorptioun-Ion-Interaktioun vun Surfaktanten op der Zell-Waasser-Interface.Ofsenkung vum cmc vun Surfaktanten féiert normalerweis zu enger méi staarker interfacial Adsorption vun Surfaktanten, wat normalerweis zu hirer erhöhter akuter Toxizitéit resultéiert.Eng Erhéijung vun der Längt vun der hydrophobescher Kette vun Surfaktanten féiert och zu enger Erhéijung vun der akuter Toxizitéit vun der Surfaktant.Déi meescht AAS sinn niddereg oder net gëfteg fir Mënschen an d'Ëmwelt (besonnesch fir Marineorganismen) a si gëeegent fir als Liewensmëttel Zutaten, Medikamenter a Kosmetik ze benotzen.Vill Fuerscher hunn bewisen datt Aminosaier Surfaktanten sanft an net irritéierend fir d'Haut sinn.Arginin-baséiert Surfaktanten si bekannt manner gëfteg wéi hir konventionell Géigeparteien.
Brito et al.studéiert déi physikalesch-chemesch an toxikologesch Eegeschafte vun Amphiphile baséiert op Aminosäuren an hir [Derivate vum Tyrosin (Tyr), Hydroxyprolin (Hyp), Serin (Ser) a Lysin (Lys)] spontan Bildung vu kationesche Vesikel an hunn Daten iwwer hir akuter Toxizitéit fir Daphnia magna (IC 50).Si hunn kationesch Vesikel vun Dodecyltrimethylammoniumbromid (DTAB)/Lys-Derivate an/oder Ser-/Lys-Derivatmëschungen synthetiséiert an hir Ökotoxizitéit an hémolytesch Potenzial getest, ze weisen datt all AAS an hir vesikelhalteg Mëschunge manner gëfteg waren wéi déi konventionell Surfaktant DTAB. .
Rosa et al.ënnersicht d'Bindung (Associatioun) vun DNA zu stabil Aminosaier Saier-baséiert kationic vesicles.Am Géigesaz zu konventionelle kationesche Surfaktanten, déi dacks gëfteg schéngen, schéngt d'Interaktioun vu kationeschen Aminosaier Surfaktanten net gëfteg ze sinn.Déi kationesch AAS baséiert op Arginin, déi spontan stabil Vesikel a Kombinatioun mat bestëmmten anionesche Surfaktanten bilden.Aminosäure-baséiert Korrosiounsinhibitoren ginn och als net-gëfteg gemellt.Dës Surfaktanten si liicht synthetiséiert mat héijer Rengheet (bis zu 99%), niddereg Käschten, liicht biologesch ofbaubar a komplett löslech an wässerleche Medien.Verschidde Studien hu gewisen datt Schwefelhalteg Aminosaier Surfaktanten superior sinn an der Korrosiounsinhibitioun.
An enger rezenter Etude, Perinelli et al.gemellt en zefriddestellend toxikologesche Profil vun Rhamnolipiden am Verglach mat konventionellen Surfaktanten.Rhamnolipiden si bekannt als Permeabilitéitsverbesserer ze handelen.Si hunn och den Effekt vun Rhamnolipiden op d'Epithelpermeabilitéit vu makromolekuläre Medikamenter gemellt.
08 Antimikrobial Aktivitéit
D'antimikrobiell Aktivitéit vun Surfaktanten kann duerch d'Mindesthemmungskonzentratioun evaluéiert ginn.D'antimikrobial Aktivitéit vun Arginin-baséiert Surfaktanten gouf am Detail studéiert.Gram-negativ Bakterien goufe méi resistent géint Arginin-baséiert Surfaktanten wéi Gram-positiv Bakterien fonnt.D'antimikrobiell Aktivitéit vun Surfaktanten gëtt normalerweis erhéicht duerch d'Präsenz vun Hydroxyl, Cyclopropan oder onsaturéierte Bindungen an den Acylketten.Castillo et al.huet gewisen datt d'Längt vun den Acylketten an déi positiv Ladung den HLB-Wäert (hydrophil-lipophile Gläichgewiicht) vun der Molekül bestëmmen, an déi hunn en Effekt op hir Fäegkeet fir Membranen ze stéieren.Nα-acylarginine Methylester ass eng aner wichteg Klass vu kationesche Surfaktanten mat breet-Spektrum antimikrobieller Aktivitéit an Et ass liicht biodegradéierbar an huet niddereg oder keng Toxizitéit.Studien iwwer d'Interaktioun vun Na-acylarginin Methylester-baséiert Surfaktanten mat 1,2-dipalmitoyl-sn-propyltrioxyl-3-phosphorylcholin an 1,2-ditetradecanoyl-sn-propyltrioxyl-3-phosphorylcholin, Modellmembranen a mat liewegen Organismen an d'Präsenz oder d'Feele vun externen Barrièren hunn gewisen datt dës Klass vun Surfaktanten gutt antimikrobiell D'Resultater weisen datt d'Surfactanten eng gutt antibakteriell Aktivitéit hunn.
09 Rheologesch Eegeschaften
Déi rheologesch Eegeschafte vun Surfaktanten spillen eng ganz wichteg Roll bei der Bestëmmung an der Viraussetzung vun hiren Uwendungen a verschiddenen Industrien, dorënner Liewensmëttel, Medikamenter, Uelegextraktioun, perséinlech Betreiung an Heemfleegprodukter.Vill Studien goufen duerchgefouert fir d'Relatioun tëscht Viskoelastizitéit vun Aminosaier Surfaktanten a cmc ze diskutéieren.
10 Uwendungen an der Kosmetikindustrie
AAS ginn an der Formuléierung vu ville perséinleche Fleegeprodukter benotzt.Kalium-N-Kokoylglycinat gëtt fonnt fir sanft op der Haut a gëtt an der Gesiichtsreinigung benotzt fir Schlamm a Make-up ze entfernen.n-Acyl-L-Glutaminsäure huet zwou Carboxylgruppen, wat et méi Waasserléislech mécht.Ënnert dësen AAS, AAS baséiert op C 12 Fettsäuren gi wäit an der Gesiichtsreinigung benotzt fir Schlamm a Make-up ze läschen.AAS mat enger C 18 Kette ginn als Emulgatoren an Hautfleegprodukter benotzt, an N-Lauryl Alanin Salze si bekannt fir cremeg Schaum ze kreéieren déi d'Haut net irritéieren an dofir an der Formuléierung vu Babyfleegprodukter benotzt kënne ginn.N-Lauryl-baséiert AAS, déi an Zahnpasta benotzt gëtt, hunn eng gutt Detergency ähnlech wéi Seife a staark Enzym-inhibitend Effizienz.
An de leschte Joerzéngte huet d'Wiel vun Surfaktanten fir Kosmetik, perséinlech Betreiungsprodukter a Medikamenter konzentréiert sech op niddereg Toxizitéit, Mëllheet, sanft fir den Touch a Sécherheet.Konsumenten vun dëse Produkter sinn akut bewosst iwwer déi potenziell Reizung, Toxizitéit an Ëmweltfaktoren.
Haut ginn AAS benotzt fir vill Shampoos, Hoerfaarwen a Badseifen ze formuléieren wéinst hire ville Virdeeler iwwer hir traditionell Géigeparteien a Kosmetik a perséinlech Betreiungsprodukter.Protein-baséiert Surfaktanten hunn wënschenswäert Eegeschafte fir perséinlech Betreiungsprodukter.E puer AAS hunn filmformende Fäegkeeten, anerer hunn gutt Schaumfäegkeeten.
Aminosaier Saieren si wichteg natierlech optriede moisturizing Faktoren am Stratum corneum.Wann Epidermalzellen stierwen, ginn se en Deel vum Stratum corneum an déi intrazellulär Proteine gi graduell zu Aminosäuren ofgebaut.Dës Aminosäuren ginn dann weider an de Stratum corneum transportéiert, wou se Fett oder fettähnlech Substanzen an den epidermale Stratum corneum absorbéieren, an domat d'Elastizitéit vun der Hautoberfläche verbesseren.Ongeféier 50% vum natierleche Feuchtigkeitfaktor an der Haut besteet aus Aminosäuren a Pyrrolidon.
Collagen, e gemeinsame kosmeteschen Zutat, enthält och Aminosäuren, déi d'Haut mëll halen.Hautprobleemer wéi Rauhheet an Dullness sinn zu engem groussen Deel wéinst engem Mangel un Aminosäuren.Eng Etude huet gewisen datt d'Mëschung vun enger Aminosäure mat enger Salbe d'Hautverbrennunge erliichtert, an déi betroffene Gebidder zréck an hiren normalen Zoustand ouni keloid Narben ze ginn.
Aminosäuren goufen och als ganz nëtzlech fonnt fir beschiedegt Kutikula ze këmmeren.Dréchen, formlos Hoer kënnen eng Ofsenkung vun der Konzentratioun vun Aminosäuren an engem schwéier beschiedegten Stratum Corneum uginn.Aminosäuren hunn d'Fähigkeit fir d'Kutikula an d'Hoerschacht ze penetréieren an d'Feuchtigkeit vun der Haut opzehuelen.Dës Fäegkeet vun Aminosäure baséiert Surfaktanten mécht se ganz nëtzlech a Shampoos, Hoerfaarwen, Hoerweichmëttel, Hoerkonditioner, an d'Präsenz vun Aminosäuren mécht d'Hoer staark.
11 Uwendungen an alldeegleche Kosmetik
De Moment gëtt et eng wuessend Nofro fir Aminosaier-baséiert Detergent Formuléierungen weltwäit.AAS si bekannt fir besser Reinigungsfäegkeet, Schaumfäegkeet a Stoffweichendungseigenschaften ze hunn, wat se gëeegent mécht fir Haushaltswäschmëttel, Shampoos, Kierperwäschen an aner Uwendungen.Eng asparaginsäure-ofgeleet amphoteresch AAS gëtt gemellt als en héich effektiven Detergent mat chelatesche Properties.D'Benotzung vun Detergent Zutaten, déi aus N-alkyl-β-aminoethoxysäuren besteet, gouf fonnt fir d'Hautreizung ze reduzéieren.Eng flësseg Detergentformuléierung besteet aus N-cocoyl-β-aminopropionat gouf gemellt als en effektiven Detergent fir Uelegflecken op Metalloberflächen.En Aminocarboxylsäure-Surfactant, C 14 CHOHCH 2 NHCH 2 COONa, gouf och bewisen fir besser Detergency ze hunn a gëtt benotzt fir Textilien, Teppecher, Hoer, Glas, asw.. D'2-Hydroxy-3-Aminopropionsäure-N,N- Acetoacetic sauerem Derivat ass bekannt fir eng gutt komplexéierend Fäegkeet ze hunn an doduerch Stabilitéit un Bleechmëttelen gëtt.
D'Virbereedung vun Detergent Formuléierungen baséiert op N-(N'-Long-chain Acyl-β-alanyl)-β-alanine gouf vum Keigo an Tatsuya an hirem Patent gemellt fir besser Wäschfäegkeet a Stabilitéit, einfach Schaumbriechung a gutt Stoffweichung. .Kao entwéckelt eng Detergentformuléierung baséiert op N-Acyl-1-N-Hydroxy-β-alanine a bericht niddereg Hautirritatioun, héich Waasserresistenz an héich Fleckenentfernungsmuecht.
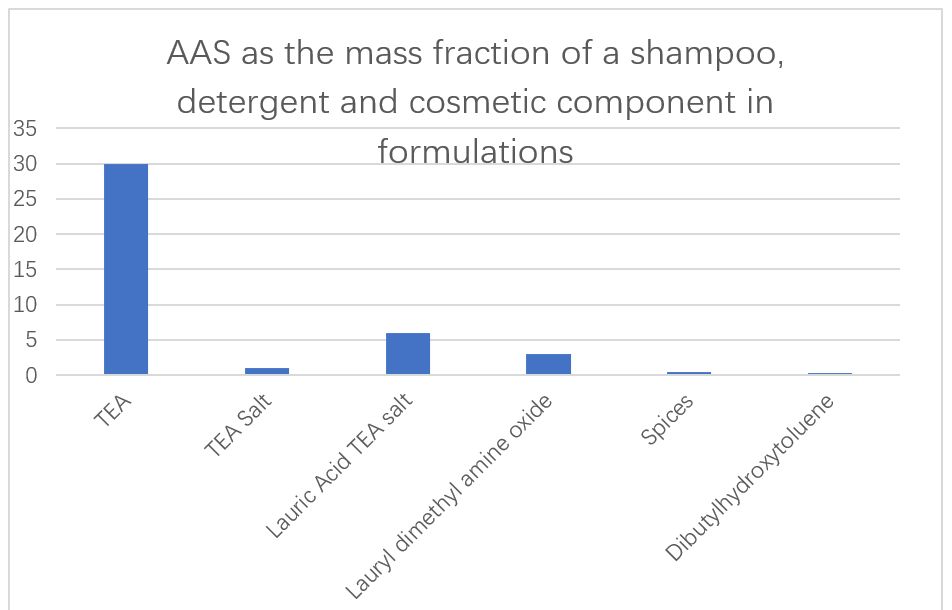
Déi japanesch Firma Ajinomoto benotzt niddereg-gëfteg a liicht ofbaubar AAS baséiert op L-Glutaminsäure, L-Arginin a L-Lysin als Haaptzutaten an Shampoos, Detergenten a Kosmetik (Figure 13).D'Fäegkeet vun Enzyminadditive an Detergentformuléierungen fir Proteinfouling ze entfernen ass och gemellt ginn.N-Acyl AAS ofgeleet vu Glutaminsäure, Alanin, Methylglycin, Serin an Asparaginsäure goufe gemellt fir hir Benotzung als exzellent flësseg Detergenten an wässerleche Léisungen.Dës Surfaktanten erhéijen d'Viskositéit guer net, och bei ganz niddregen Temperaturen, a kënne ganz einfach aus dem Späicherbehälter vum Schaumgerät transferéiert ginn fir homogene Schaum ze kréien.
Post Zäit: Jun-09-2022

